Hovedbudskap
Kognitiv svikt ved schizofreni er vanlig og er stabil gjennom livet hos de fleste med sykdommen.
En liten andel opplever progredierende kognitiv svikt med økende alder og utvikler demens.
Livstilsfaktorer er av betydning for demensutvikling og fokus på disse kan forhåpentligvis bidra til å redusere risiko for demens ved schizofreni
Forfattet av
Cecilie Bhandari Hartberg
Utdannet Cand.med ved Universitet i Oslo i 2003. Ph.d. ved UiO i 2011 og spesialist i psykiatri i 2016.
Overlege ved enhet for psykosomatikk/CL-voksen, Rikshospitalet, Klinikk for psykisk helse og avhengighet, OUS.
Epost: c.b.hartberg@medisin.uio.no
Artikkelen til nedlasting
Introduksjon
Schizofreni ble først beskrevet av den tyske psykiateren Kraepelin, som omtalte lidelsen som Dementia Praecox (1). Han mente at kognitiv fungering ble forverret etter hvert som schizofrenilidelsen progredierte og, som navnet antyder, mente han at sykdommen førte til tidlig demens. Symptomene ved schizofreni kan deles inn i positive og negative symptomer. De positive symptomene er for eksempel vrangforestillinger, hallusinasjoner og tankeforstyrrelser, mens eksempler på negative symptomer er at en person er følelsesmessig flat, likegyldig, gledesløs, mangler ansiktsmimikk og strever med konsentrasjonen. I tillegg er det vist at så mange som 75 prosent av de med schizofreni har redusert kognitiv funksjon på ett eller flere områder (2).
Schizofreni er en sykdom som oftest rammer i ungdomstid eller tidlig i voksenlivet. Selv om sykdommen er relativt sjeldent forekommende får den store konsekvenser for den enkelte person og for samfunnet. Det er en hyppig årsak til at man faller ut av arbeid og får tidlig uføretrygd (3). Schizofreni er en sykdom som hos de fleste gir symptomer i perioder av livet. Til tross for at man har perioder med lettere eller ingen psykosesymptomer er det mange som syns det er vanskelig å arbeide. Den nedsatte evnen til å fungere i arbeidslivet skyldes til en viss grad kognitive vansker (4) . De siste tiårene har forskning avdekket at de kognitive vanskene er tilstede allerede når sykdommen oppstår, og at de kan prege hverdagen i stor grad (5). Man har imidlertid hatt lite kunnskap om hvordan den kognitive fungeringen utvikler seg i et livsperspektiv og om det er økt risiko for å få demens ved schizofreni. I det følgende presenteres et subjektivt utvalg av studier som er gjort på dette området basert på relevans. For å begrense litteraturlisten omtales flere metaanalyser og oversiktsartikler.
Normal kognitiv aldring
Kognisjon er en samlebetegnelse som brukes om de mentale prosessene som inngår i tankevirksomheten vår. Kognitive funksjoner omfatter blant annet å tenke, huske, lære, gjenkalle, oppfatte og vurdere kunnskap eller informasjon om miljøet og å reagere på omgivelsene. Det er vanlig å bruke kartleggingsverktøy, som MMSE og klokketest i demensutredning ved alderspsykiatriske og geriatriske avdelinger for å vurdere om det finnes en kognitiv svikt, og om den progredierer over tid. Fagpersoner, som nevropsykologer, kan ved hjelp av samtale, observasjon og bruk av nevropsykologiske tester gjøre en bredere vurdering av kognitiv funksjon. Det er flere måter å kategorisere de ulike kognitive funksjonene på. Innenfor schizofreniforskning har man de siste årene forsøkt å samle seg om å bruke et testbatteri basert på konsensus fra MATRICS (Measurement and Treatment Research to Improve Cognition in Schizophrenia) (6), som er utarbeidet i USA. Det MATRICS-baserte testbatteriet kartlegger syv utvalgte kognitive kategorier (Tekstboks 1). Man har også inkludert et område som kalles sosial kognisjon, som undersøker evnen til å forstå og tolke sosial informasjon, oppfatte og tolke andres emosjonelle uttrykk og forstå og reagere i henhold til sosiale normer.
For å finne ut om kognitiv fungering endrer seg over tid, for eksempel etter en periode med legemiddelbehandling eller ved aldring, er det nødvendig å undersøke samme person flere ganger. Testene som inngår i dette batteriet skal i mindre grad være sensitive for læringseffekt, slik at man kan undersøke samme person flere ganger uten at det påvirker resultatene, men retesting vil nok alltid være forbundet med en viss grad av læring.

Det er også utfordrende å måle rene alderseffekter med tanke på at alderdommen er forbundet med sykdommer, som Alzheimers demens, Parkinsons, hypertensjon og diabetes, som kan påvirke hjernen og dermed kognitiv funksjon. Det er likevel gjort undersøkelser av selekterte og friske personer, som har vist at aldring er forbundet med visse forandringer.
Med unntak av prosesseringshastighet som synker gradvis gjennom hele voksenlivet, vil de fleste friske oppleve en stabilitet av kognitive funksjoner fram til 40- 50 årsalder, før det tilkommer en gradvis reduksjon. Kognitive funksjoner som involverer godt innøvede oppgaver eller er kunnskapsbaserte er oftest bevart til sent i livet. Et eksempel på dette er språkkunnskap og ordforråd. Det er verdt å nevne at sosial kognisjon og fokus på emosjonelle mentale aspekter vedvarer hos eldre (7).
Kognitiv utvikling og svikt ved schizofreni
På bakgrunn av Kraepelins beskrivelser av sykdomsprogresjon trodde man lenge at schizofreni var en rent nevrodegenerativ sykdom. De første studiene som benyttet billedundersøkelser av hjernen støttet også den teorien. I 1976 publiserte Eve Johnstone en CT-studie av 18 menn med schizofreni, som viste nedsatt global kognitiv fungering, samtidig med forstørrede hulrom (hjerneventrikler), som tydet på reduksjon av hjernestruktur og -funksjon (8). At schizofreni gir en form for tidlig demens eller fører til tidlig eller akselerert aldring, kan også være en plausibel teori med tanke på andre forhold ved sykdommen. De som har schizofreni har større risiko for tidlig død på grunn av uheldig livsstil, diabetes, mellitus, kreft og kardiovaskulær sykdom, og man finner delte risikofaktorer mellom schizofreni og aldersrelaterte tilstander, som for eksempel høy alder hos far, lav fødselsvekt og spesifikke gener. Senere ble det publisert studier som hadde fulgt pasienter over lang tid (gjennomsnittlig 37 år), og som fremstilte et mye mer nyansert bilde (9). En del personer klarte seg bra med hensyn til sosial funksjon til tross for vedvarende positive psykotiske symptomer, mens funksjonen til andre kunne forverres uten at tydelige symptomer var tilstede. Kun en liten andel på åtte prosent ble diagnostisert med demensliknende tilstander (9). Det er dessuten ikke funnet noen form for organisk sykdom eller skade i hjernen som er ensbetydende med schizofreni og som man kan finne ved andre nevrodegenerative sykdommer. Sykdommen er kategorisert som en ikke-organisk lidelse i diagnosesystemene ICD-10 og DSM-V.
Senere ble det publisert studier som hadde fulgt pasienter over lang tid (gjennomsnittlig 37 år), og som fremstilte et mye mer nyansert bilde
De siste tiårene har schizofreniforskningen dreid fokuset mot utviklingen av nervesystemet fra fødsel til sykdommen manifesterer seg i voksenlivet. På slutten av 80-tallet ble «nevroutviklingshypotesen» lansert (10) og i de påfølgende årene ble det publisert mange vitenskapelige studier som støtter at det foreligger en forstyrrelse i utviklingen tidlig i livet ved schizofreni. Blant annet er det vist at mange som får schizofreni har kognitive vansker allerede før de kommer til behandling første gang, noe som tyder på at den kognitive svikten oppstår før symptomene blir tydelige for en selv og andre (11). I årene etter sykdomsdebut er den kognitive fungeringen lavere enn hos friske, men relativt stabil (11).
Tilsvarende har man funnet stabil fungering over en femårsperiode blant personer med kronisk schizofreni i 40-50 årene (12). Siden personer med schizofreni ofte har en vedvarende kognitiv svikt er det av interesse om utviklingen følger den man ser hos friske eldre, som har en gradvis reduksjon i kognitiv fungering etter 50-60 års alder, eller om de opplever en raskere progresjon av kognitiv svikt. En meta-analyse av eldre personer (gjennomsnittlig 65 år gamle) sammenfattet resultatene fra 29 tverrsnittsstudier og 14 longitudinelle studier med oppfølgingstid mellom ett og seks år (13). Sammenfatningen konkluderte med betydelig og generell kognitiv reduksjon i denne gruppen, men konkluderte med at det ikke forelå signifikant kognitiv endring over tid. En annen oversiktsartikkel konkluderte imidlertid med at det var tegn til kognitiv reduksjon over tid. Blant de 20 studiene som var inkludert, var det tolv studier som antydet kognitiv reduksjon over tid, mens åtte studier fant ingen endring over tid (14). Forskjellene mellom studiene skyldes sannsynligvis forskjeller mellom deltakerne i studiene, for det er klare metodiske utfordringer når man skal undersøke personer som har levd med sykdom over tid. Flere forhold ved sykdomsforløpet, behandlingen og livsstilen kan påvirke den kognitive utviklingen.
Demensutvikling
Demens er en samlebetegnelse på kognitiv svikt og funksjonsendring som følge av organiske sykdommer eller skader. Alzheimers sykdom er den hyppigst årsaken til demens, men det finnes flere årsaker. Ulike metoder har blitt benyttet for å undersøke forekomsten av demens ved schizofreni.
Forskerne bak en nevropatologisk studie av 100 pasienter med schizofreni, undersøkte først kognitiv funksjon og konkluderte med at 72 prosent av pasientene hadde moderat til alvorlig kognitiv reduksjon. Pasientene ble senere obdusert og man fant at kun ni prosent oppfylte de nevropatologiske kriterier for Alzheimers sykdom. Det vil si at Alzheimers sykdom som hovedregel ikke var årsaken til den kognitive svikten som personene hadde (15).
En dansk registerstudie fra 2003 undersøkte forekomsten av demensdiagnoser hos de som har schizofrenidiagnose fra tidligere. Av omkring 2,8 millioner mennesker var det 0,7 prosent som hadde diagnosen schizofreni. I diagnoseregistrene 18 år senere fant man dobbelt så ofte demenslidelse hos de med schizofrenidiagnose sammenliknet med friske. Det er verdt å merke seg at risikoøkningen var mest uttalt for de under 65 år og mindre dersom man korrigerte for rusbruk. Ifølge registerstudien var absolutt risiko for demensdiagnose 0,6 prosent for tidligere friske kontroller, mens den var 1,8 prosent for de med tidligere schizofrenidiagnose (16).
Resultatene fra en nylig publisert meta-analyse som har vurdert resultatene fra seks studier, deriblant den danske registerstudien, er i tråd med de danske resultatene og viser en relativ risiko på 2,3 prosent for demensdiagnose ved schizofreni (17), men forfatterne av meta-analysen mente de enkelte studiene ga for lite informasjon om subgrupper til å avgjøre om hvilke typer demens risikoen var økt for.
Utrede og diagnostisere demensutvikling
Å diagnostisere demens ved schizofreni byr på en rekke utfordringer. Det kan være vanskelig å skille mellom eksisterende og langvarig kognitiv svikt fra en nyoppstått demensutvikling. Dessuten kan negative symptomer og legemiddelbivirkninger bidra til ytterligere vansker, for eksempel ved at personen har redusert psykomotorisk tempo og dermed oppfattes å ha kognitiv dysfunksjon. En samtale med pasienten og en pårørende eller omsorgsperson bør ha fokus på omfanget av tidligere kognitiv svekkelse og funksjonsnivå. Dersom kognitiv fungering svinger med grad av psykotiske symptomer er demensutvikling mindre sannsynlig. Dersom den kognitive fungeringen blir gradvis redusert er demensutvikling mer sannsynlig. Videre bør man foreta en gjennomgang av hvilke antipsykotiske legemidler som benyttes, dosering og serumkonsentrasjon. Ved økt alder kan det være hensiktsmessig å redusere dose av legemidler på grunn av endring i farmakokinetiske forhold.
Ved bruk av strukturerte metoder bør man velge flere verktøy slik at man kartlegger et bredt spekter av kognitiv funksjon, blant annet eksekutiv fungering, og negative psykotiske symptomer. Noen anbefalte strukturerte intervjuer (18) med kommentarer finnes i tabell 1. Flere av intervjuene bør utføres og fortolkes i samarbeid med nevropsykolog.

Som ved andre psykiske lidelser benyttes CT og MR caput for å utelukke hjerneorganisk årsak til kognitiv svikt, men strukturelle hjerneforandringer er ikke spesifikke for schizofreni, Alzheimers sykdom eller vaskulær demens og kan dermed ikke brukes til å stille demensdiagnose ved schizofreni. Ved schizofreni er forstørrede sideventrikler det vanligste funnet, mens ved demens er hjerneatrofi og småkarforandringer vanlige funn. De omtalte hjerneforandringene kan også forekomme hos friske, eldre mennesker.
Diagnosen stilles på bakgrunn av kriteriene for demens dersom det foreligger en endring i kognitiv funksjon og dagliglivsfunksjon og man ikke finner annen årsak til endring. Dersom man har resultater fra tidligere utført kognitiv utredning og billedundersøkelser, er de svært nyttige i en pågående utredning slik at man vurdere om det har forekommet en progresjon. Alternativt kan man avtale at pasienten gjennomfører en ny undersøkelse etter ett år, for å avdekke om det foreligger en progredierende tilstand.
Behandling av kognitiv svikt eller demens
Schizofreni behandles med antipsykotiske legemidler, noe som kan forbedre kognitiv funksjon dersom den kognitive svikten er forbundet med psykotiske symptomer. Legemidlene har liten eller ingen effekt på kognitiv svikt som er uavhengig av symptomene, det vil si som er tilstede i symptomfrie faser (20). Det er gjort en rekke studier for å undersøke effekten av målrettet kognitiv trening. Treningen består av vitenskapelige prinsipper for læring for å øke kognitive prestasjoner på de områdene som svikter, for eksempel oppmerksomhet, hukommelse, eksekutiv og sosial funksjon. Helst bør treningen utføres i den sammenhengen personen har bruk for den, for eksempel på skole eller i arbeid. Kognitiv trening har vist seg å ha en liten, men varig effekt på hukommelse og oppmerksomhet ved schizofreni (21).
Det finnes ingen retningslinjer for behandling av nyoppstått demens ved schizofreni. Man har nokså god dokumentasjon på at man skal være varsom med bruk av antipsykotiske legemidler for å behandle psykose som tilleggssymptomer ved demens på grunn av økt risiko for hjerneslag og ekstrapyramidale symptomer (22), men det er usikkert om denne risikoen er økt hos personer som har schizofreni fra tidligere eller om bruk av demenslegemidler kan forbedre kognitiv funksjon. Det er ingen kunnskapsoppsummering på dette feltet, men det finnes noen enkeltstudier som har vist lovende resultater. Det mangler studier som undersøker langtidseffekten av å legge til demenslegemidler. De få studiene som er utført antyder at acetylkolinesterasehemmere i kombinasjon med antipsykotiske legemidler kan ha en positiv effekt på negative symptomer, depresjon og kognisjon (23).
Diskusjon
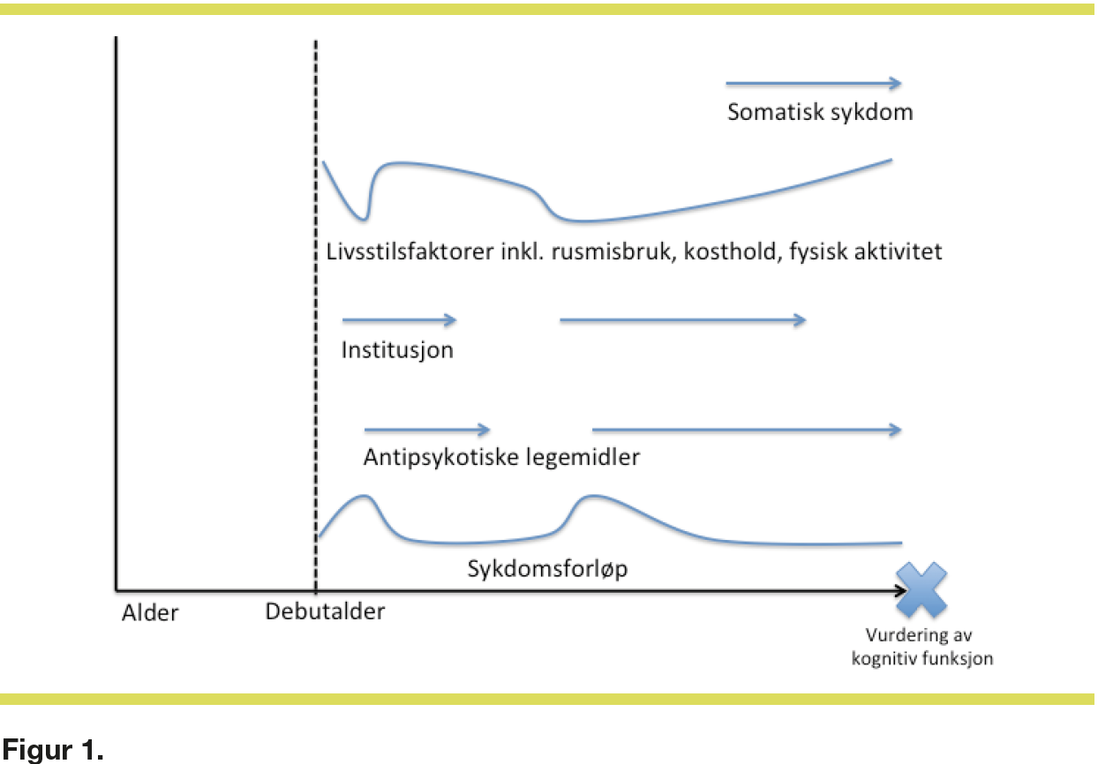
For den andelen som opplever progresjon av kognitiv svikt eller får en demenslidelse er det vanskelig å vurdere om det er schizofrenilidelsen i seg selv som progredierer eller om det er andre forhold som påvirker, for eksempel alder ved debut av sykdom, sykdomsforløp, legemiddelbehandling, institusjonsopphold, livsstilsfaktorer og somatisk sykdom (Figur 1).
En studie fra 1994 undersøkte om alder ved debut av sykdom hadde effekt på kognitiv svikt. Kognitiv funksjon hos en gruppe med unge schizofrenipasienter ble sammenliknet med eldre pasienter. De eldre pasientene ble igjen delt inn i to grupper med henholdsvis tidlig og sen debut etter 45 års alder. De konkluderte med at kognitiv svekkelse ved schizofreni ikke er knyttet til nåværende alder, debutalder eller varighet av sykdom (24). Oversiktsartikkelen av Shah et al (14), fant heller ingen forskjell mellom de som ble syke i ung alder og de som ble syke sent.
Når det gjelder om alvorlighetsgrad av symptomer og sykdomsforløp påvirker kognitiv utvikling, ble dette undersøkt i en finsk studie. De finske forskerne har fulgt en kohort av pasienter over mange år. Deres undersøkelser konkluderte med at symptomgrad ikke var forbundet med påfølgende kognitiv reduksjon, men at utdannelse og skoleprestasjoner spilte en betydelig rolle for kognitiv funksjon senere i livet (25).
Flere av de studiene som har funnet holdepunkter for progresjon av kognitiv svikt hos eldre personer, har inkludert mennesker som har bodd eller oppholdt seg på institusjon i lange perioder (26, 27). Personene kan ha blitt påvirket av oppholdet og blitt lite stimulert. Det motsatte er også mulig. At personer som har progredierende sykdom i større grad har behov for lange institusjonsopphold enn andre (28).
Da andregenerasjons antipsykotika ble lansert var det knyttet forventinger til at de kunne virke positivt på kognisjon, men selv om kognitiv fungering kan forbedres noe på grunn av symptomlette etter oppstart, er det vanligvis beskjedne forbedringer ved langvarig behandling (20, 29). Det er dessuten lite evidens for at langsiktig behandling med antipsykotisk legemidler kan forhindre utviklingen av demens ved schizofreni.
Høyere forekomst av rusmisbruk, dårlig kosthold, somatisk sykdom og lite fysisk aktivitet blant personer med schizofreni gjør denne pasientgruppen mer utsatt for kognitiv svikt og demensutvikling. Samlet sett synes det som institusjonsopphold og livsstil har mer betydning for den kognitive utviklingen enn sykdomsforløp og medikamentell behandling, og bør tas med i betraktning når man fortolker forskningen om utvikling av kognitiv funksjon ved schizofreni. Det er lite som tyder på at det å ha sykdommen schizofreni i seg selv automatisk fører til progresjon av kognitiv svikt når man blir eldre, men en viss andel kan, på grunn av livsstil eller genetiske faktorer, være mer utsatt for en negativ utvikling.
Utredningen av demens ved schizofreni kan være utfordrende hvis man ikke kjenner til tidligere kognitiv funksjon og utvikling. En eksisterende svikt kan ha vært langvarig og kan feilaktig bedømmes til å være tegn på demensutvikling. Samtidig kan man overse behovet for utredningen ved mulig sykdomsprogresjon hos de som har en kjent svikt fra tidligere eller har lav funksjon. Som helsepersonell kan man risikere både å over- og underdiagnostisere demens ved schizofreni.
Det er uansett viktig å ha fokus på kognitiv svikt og mulig progresjon. Ikke alle har kognitiv svikt, men det er likevel så vanlig forekommende ved schizofreni at man som helsepersonell bør ta det med i betraktning når man planlegger utredning, behandling og rehabilitering. Kognitive vansker kan ha betydning for i hvilken grad man benytter seg av helsetjenester og for behandlingsforløpet. Helt siden sykdommen ble beskrevet første gang har man visst at kognitive vansker er en del av sykdomsbildet, men det er først de senere årene man har kartlagt hvor tidlig plagene er tilstede og hvilke konsekvenser de får. Forebyggende tiltak som vekt- og blodtrykkskontroll, fokus på blodsukkerstigning, fysisk trening, motivasjon for røykeslutt og behandling av rusmisbruk kan forhåpentligvis redusere risiko for å utvikle demens.
Konklusjon
Sammenfattet kan man si at kognitiv svikt er vanlig ved schizofreni allerede ved sykdomsdebut. Det er fortsatt stor usikkerhet knyttet til om den kognitive svikten progredierer, men det kan se ut til at en liten andel opplever tidlig kognitiv reduksjon, som ved demens. Risikoen for å få demensdiagnose ved schizofreni er doblet sammenliknet med øvrig befolkning. Hos helsepersonell er det viktig å være oppmerksom på mulig progresjon og demensutvikling, slik at man kan gi tilpasset omsorg til de som rammes.
Referanser
- Kraepelin E. Dementia Praecox and Paraphrenia. New York: Robert E. Krieger Publishing Co; 1917 1917.
- Palmer BW, Dawes SE, Heaton RK. What do we know about neuropsychological aspects of schizophrenia? Neuropsychol Rev. 2009;19(3):365-84.
- Evensen S, Wisloff T, Lystad JU, Bull H, Ueland T, Falkum E. Prevalence, Employment Rate, and Cost of Schizophrenia in a High-Income Welfare Society: A Population-Based Study Using Comprehensive Health and Welfare Registers. Schizophr Bull. 2016;42(2):476-83.
- Lystad JU, Falkum E, Haaland VO, Bull H, Evensen S, Bell MD, et al. Neurocognition and occupational functioning in schizophrenia spectrum disorders: The MATRICS Consensus Cognitive Battery (MCCB) and workplace assessments. Schizophr Res. 2016;170(1):143-9.
- Mesholam-Gately RI, Giuliano AJ, Goff KP, Faraone SV, Seidman LJ. Neurocognition in first-episode schizophrenia: a meta-analytic review. Neuropsychology. 2009;23(3):315-36.
- Nuechterlein KH, Green MF, Kern RS, Baade LE, Barch DM, Cohen JD, et al. The MATRICS Consensus Cognitive Battery, part 1: test selection, reliability, and validity. AmJPsychiatry. 2008;165(2):203-13.
- Hedden T, Gabrieli JD. Insights into the ageing mind: a view from cognitive neuroscience. Nat Rev Neurosci. 2004;5(2):87-96.
- Johnstone EC, Crow TJ, Frith CD, Husband J, Kreel L. Cerebral ventricular size and cognitive impairment in chronic schizophrenia. Lancet. 1976;2(7992):924-6.
- Ciompi L. Catamnestic long-term study on the course of life and aging of schizophrenics. Schizophr Bull. 1980;6(4):606-18.
- Murray RM, Lewis SW. Is schizophrenia a neurodevelopmental disorder? BrMedJ(ClinResEd). 1987;295(6600):681-2.
- Bora E, Murray RM. Meta-analysis of cognitive deficits in ultra-high risk to psychosis and first-episode psychosis: do the cognitive deficits progress over, or after, the onset of psychosis? Schizophr Bull. 2014;40(4):744-55.
- Ekerholm M, Firus Waltersson S, Fagerberg T, Soderman E, Terenius L, Agartz I, et al. Neurocognitive function in long-term treated schizophrenia: a five-year follow-up study. Psychiatry Res. 2012;200(2-3):144-52.
- Irani F, Kalkstein S, Moberg EA, Moberg PJ. Neuropsychological performance in older patients with schizophrenia: a meta-analysis of cross-sectional and longitudinal studies. Schizophr Bull. 2011;37(6):1318-26.
- Shah JN, Qureshi SU, Jawaid A, Schulz PE. Is there evidence for late cognitive decline in chronic schizophrenia? Psychiatr Q. 2012;83(2):127-44.
- Purohit DP, Perl DP, Haroutunian V, Powchik P, Davidson M, Davis KL. Alzheimer disease and related neurodegenerative diseases in elderly patients with schizophrenia: a postmortem neuropathologic study of 100 cases. Arch Gen Psychiatry. 1998;55(3):205-11.
- Ribe AR, Laursen TM, Charles M, Katon W, Fenger-Gron M, Davydow D, et al. Long-term Risk of Dementia in Persons With Schizophrenia: A Danish Population-Based Cohort Study. JAMA Psychiatry. 2015;72(11):1095-101.
- Cai L, Huang J. Schizophrenia and risk of dementia: a meta-analysis study. Neuropsychiatr Dis Treat. 2018;14:2047-55.
- Radhakrishnan R BR, Head L. Dementia in Schizophrenia. Advances in psychiatric treatment. 2012;18:144-53.
- Bowie CR, Harvey PD, Moriarty PJ, Parrella M, White L, Mohs RC, et al. Cognitive assessment of geriatric schizophrenic patients with severe impairment. Arch Clin Neuropsychol. 2002;17(7):611-23.
- Nielsen RE, Levander S, Kjaersdam Telleus G, Jensen SO, Ostergaard Christensen T, Leucht S. Second-generation antipsychotic effect on cognition in patients with schizophrenia–a meta-analysis of randomized clinical trials. Acta Psychiatr Scand. 2015;131(3):185-96.
- Wykes T, Huddy V, Cellard C, McGurk SR, Czobor P. A meta-analysis of cognitive remediation for schizophrenia: methodology and effect sizes. Am J Psychiatry. 2011;168(5):472-85.
- Ballard C, Waite J. The effectiveness of atypical antipsychotics for the treatment of aggression and psychosis in Alzheimer’s disease. Cochrane Database Syst Rev. 2006(1):CD003476.
- Singh J, Kour K, Jayaram MB. Acetylcholinesterase inhibitors for schizophrenia. Cochrane Database Syst Rev. 2012;1:CD007967.
- Heaton R, Paulsen JS, McAdams LA, Kuck J, Zisook S, Braff D, et al. Neuropsychological deficits in schizophrenics. Relationship to age, chronicity, and dementia. Archives of General Psychiatry. 1994;51(6):469-76.
- Rannikko I, Murray GK, Juola P, Salo H, Haapea M, Miettunen J, et al. Poor premorbid school performance, but not severity of illness, predicts cognitive decline in schizophrenia in midlife. Schizophr Res Cogn. 2015;2(3):120-6.
- Harvey PD, Silverman JM, Mohs RC, Parrella M, White L, Powchik P, et al. Cognitive decline in late-life schizophrenia: a longitudinal study of geriatric chronically hospitalized patients. Biol Psychiatry. 1999;45(1):32-40.
- Friedman JI, Harvey PD, Coleman T, Moriarty PJ, Bowie C, Parrella M, et al. Six-year follow-up study of cognitive and functional status across the lifespan in schizophrenia: a comparison with Alzheimer’s disease and normal aging. Am J Psychiatry. 2001;158(9):1441-8.
- Harvey PD, Reichenberg A, Bowie CR. Cognition and aging in psychopathology: focus on schizophrenia and depression. Annual Review of Clinical Psychology. 2006;2:389-409.
- Keefe RS. The longitudinal course of cognitive impairment in schizophrenia: an examination of data from premorbid through posttreatment phases of illness. J Clin Psychiatry. 2014;75 Suppl 2:8-13.

